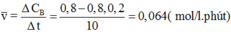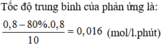Cho phản ứng: A+2B->C. Nồng độ ban đầu của A là 0.8 mol/l, của B là 1 mol/l. Sau 10 phút, nồng độ của B còn 0.6 mol/l. Vậy nồng độ của A còn lại là: A. 0.4. B. 0.2. C. 0.6. D. 0.8.

Những câu hỏi liên quan
Cho phản ứng: A + B
→
C. Nồng độ ban đầu của A là 0,12 mol/l; của B là 0,1 mol/l. Sau 10 phút, nồng độ của B giảm xuống còn 0,078 mol/l. Nồng độ còn lại (mol/1) của chất A là: A. 0,042 mol/l. B. 0,098 mol/l. C. 0,02 mol/l. D. 0,034 mol/l.
Đọc tiếp
Cho phản ứng: A + B → C. Nồng độ ban đầu của A là 0,12 mol/l; của B là 0,1 mol/l. Sau 10 phút, nồng độ của B giảm xuống còn 0,078 mol/l. Nồng độ còn lại (mol/1) của chất A là:
A. 0,042 mol/l.
B. 0,098 mol/l.
C. 0,02 mol/l.
D. 0,034 mol/l.
Chọn B.
Nồng độ chất B mất đi là: 0,1 - 0,078 = 0,022M.
Vì tỉ lệ mol là 1 : 1 nên nồng độ chất A mất đi là 0,022M.
Vậy nồng độ chất A còn lại là 0,12 - 0,022 = 0,098M.
Đúng 0
Bình luận (0)
Cho phản ứng: A + B D C Nồng độ ban đầu của A là 0,1 mol/1, của B là 0,8 mol/l. Sau 10 phút, nồng độ của B chỉ còn 20% nồng độ ban đầu. Tốc độ trung bình của phản ứng là: A. 0,16 mol/l.phút B. 0,016 mol/l.phút C. 0,064 mol/l.phút D. 0,106 mol/l.phút
Đọc tiếp
Cho phản ứng: A + B D C
Nồng độ ban đầu của A là 0,1 mol/1, của B là 0,8 mol/l. Sau 10 phút, nồng độ của B chỉ còn 20% nồng độ ban đầu. Tốc độ trung bình của phản ứng là:
A. 0,16 mol/l.phút
B. 0,016 mol/l.phút
C. 0,064 mol/l.phút
D. 0,106 mol/l.phút
Cho phản ứng: A + B D C Nồng độ ban đầu của A là 0,1 mol/1, của B là 0,8 mol/l. Sau 10 phút, nồng độ của B chỉ còn 20% nồng độ ban đầu. Tốc độ trung bình của phản ứng là: A. 0,16 mol/l.phút B. 0,016 mol/l.phút C. 0,064 mol/l.phút D. 0,106 mol/l.phút
Đọc tiếp
Cho phản ứng: A + B D C
Nồng độ ban đầu của A là 0,1 mol/1, của B là 0,8 mol/l. Sau 10 phút, nồng độ của B chỉ còn 20% nồng độ ban đầu. Tốc độ trung bình của phản ứng là:
A. 0,16 mol/l.phút
B. 0,016 mol/l.phút
C. 0,064 mol/l.phút
D. 0,106 mol/l.phút
Đáp án C
Tốc độ trung bình phản ứng:
v ¯ = ∆ C B ∆ t = 0 , 8 - 0 , 8 . 0 , 2 10 = 0 , 064 ( mol / l . phut )
Đúng 0
Bình luận (0)
Cho phản ứng hóa học: A + B → C
Nồng độ ban đầu của A là 1 mol/l, của B là 0,8 mol/l. Sau 10 phút, nồng độ của B chỉ còn 20% nồng độ ban đầu. Tốc độ trung bình của phản ứng là
A. 0,16 mol/l.phút
B. 0,016 mol/l/phút
C. 1,6 mol/l.phút
D. 0,064 mol/l.phút
Chọn D
Tốc độ trung bình của phản ứng tính theo chất B là:
![]()
Đúng 0
Bình luận (0)
Cho phản ứng
A
+
B
⇄
C
. Nồng độ ban đầu của chất A là 0,1 mol/l, của chất B là 0,8 mol/l. Sau 10 phút, nồng độ của B giảm 20% so với nồng độ ban đầu. Tốc độ trung bình của phản ứng là: A. 0,16 mol/l.phút B. 0,016 mol/l.phút C. 1,6 mol/l.phút D. 0,106 mol/l.phút
Đọc tiếp
Cho phản ứng A + B ⇄ C . Nồng độ ban đầu của chất A là 0,1 mol/l, của chất B là 0,8 mol/l. Sau 10 phút, nồng độ của B giảm 20% so với nồng độ ban đầu. Tốc độ trung bình của phản ứng là:
A. 0,16 mol/l.phút
B. 0,016 mol/l.phút
C. 1,6 mol/l.phút
D. 0,106 mol/l.phút
Hòa tan hết 9.4 g Kalioxit vào nước thu được 500 ml dung dịch X. Nồng độ mol/l của dung dịch X là:
A. 0.8 M
B. 0.6 M
C. 0.4 M
D. 0.2 M
\(n_{K_2O}=\dfrac{9.4}{94}=0.1\left(mol\right)\)
\(K_2O+H_2O\rightarrow2KOH\)
\(0.1.........................0.2\)
\(C_{M_{KOH}}=\dfrac{0.2}{0.5}=0.4\left(M\right)\)
\(C\)
Đúng 1
Bình luận (0)
Ta có: \(n_{K_2O}=\dfrac{9,4}{94}=0,1\left(mol\right)\)
PTHH: K2O + H2O ---> 2KOH
Theo PT: \(n_{KOH}=2.n_{K_2O}=2.0,1=0,2\left(mol\right)\)
\(\Rightarrow C_{M_{KOH}}=\dfrac{0,2}{500:1000}=0,4M\)
Chọn C
Đúng 0
Bình luận (0)
Cho phản ứng A+B ----> C
Nồng độ ban đầu của A là 0,1 M và của B là 0,8 M. Sau 10 phút nồng độ của B chỉ còn lại 20%
nồng độ chất ban đầu. Tốc độ trung bình của phản ứng trong khoảng thời gian đó là:
A. 0,16 mol/l.phút B. 0,016mol/l.phút C. 1,6mol/l.phút D. 0,106mol/l.phút
Cho phản ứng:
B
r
2
+
H
C
O
O
H
→
2
H
B
r
+
C
O
2
Nồng độ ban đầu của
B
r
2
là a mol/lít, sau 50 giây nồng độ
B
r
2
còn lại là 0,01 mol/lít. Tốc độ trung bình của phản ứng trên tính...
Đọc tiếp
Cho phản ứng:
B r 2 + H C O O H → 2 H B r + C O 2
Nồng độ ban đầu của B r 2 là a mol/lít, sau 50 giây nồng độ B r 2 còn lại là 0,01 mol/lít. Tốc độ trung bình của phản ứng trên tính theo B r 2 là 4 . 10 - 5 m o l ( l í t . s ) - 1 . Giá trị của a là
A. 0,018
B. 0,016
C. 0,012
D. 0,014
C
a = 4 . 10 - 5 . 50 + 0 , 01 = 0 , 012 mol/lít
Đúng 0
Bình luận (0)
Cho phản ứng Br2 + HCOOH → 2HBr + CO2 Nồng độ ban đầu của Br2 là a mol/ lít, sau 50 giây nồng độ Br2 còn lại là 0,01 mol/ lít. Tốc độ trung bình của phản ứng trên tính theo Br2 là 4.10-5 mol/ (l.s). Giá trị của a là A. 0,016 B. 0,014 C. 0,018 D. 0,012
Đọc tiếp
Cho phản ứng Br2 + HCOOH → 2HBr + CO2
Nồng độ ban đầu của Br2 là a mol/ lít, sau 50 giây nồng độ Br2 còn lại là 0,01 mol/ lít. Tốc độ trung bình của phản ứng trên tính theo Br2 là 4.10-5 mol/ (l.s). Giá trị của a là
A. 0,016
B. 0,014
C. 0,018
D. 0,012
Đáp án : D
Tốc độ v = - (C2 – C1)/t
=> C1 = 0,012 mol/lit
Đúng 0
Bình luận (0)